


想象一下,一场突如其来的中风,让原本灵巧的手脚变得不听使唤,甚至连简单的抓握都成了奢望。对于无数中风幸存者来说,这是不得不面对的残酷现实。虽然发病后的最初几周是恢复的黄金期,但仍有超过50%的患者在6个月后遗留肢体无力,尤其是上肢功能的恢复,常在3-6个月后进入平台期,改善空间有限。
有没有一种方法能突破这个瓶颈?一种名为强制性运动疗法(CIMT)的康复手段,或许能带来新的希望。简单来说,CIMT就是反复强制患者使用受损更严重的患侧肢体。
几项高质量研究已经证实CIMT的有效性,但它究竟如何在大脑层面发挥作用,尤其是在大面积脑损伤后,其背后的神经重塑机制一直是谜。今天,我们就来解读一项发表于《Behavioural Neurology》期刊的研究,看看科学家们是如何通过大鼠实验,揭示了CIMT促进中风后运动功能恢复的一个秘密:调动大脑深处一个名为“红核(RN)”的结构,并强化其与大脑皮层的连接。
当大脑皮层这个“最高司令部”受损后,身体需要寻找替代路径来传达指令。近年来,研究者们发现,一些远离梗死灶的区域,如对侧(健侧)大脑半球、皮层下结构,甚至脑干,都在恢复过程中扮演着重要角色。其中,位于中脑的红核引起了研究者的浓厚兴趣。它是红核脊髓束(RST)的起源,这条神经通路与更为人熟知的皮质脊髓束(CST)在功能上密切相关,主要负责抓握、运动控制和协调。
此前有研究显示,在小范围的脑损伤中,受损同侧的皮层-红核通路会发生变化。但是,对于大面积脑卒中,红核、尤其是双侧红核及其与双侧运动皮层的连接会发生怎样的改变?CIMT治疗是否会影响到它们?这正是本文介绍的研究希望去探索的。
为了探究上述问题,研究者们设计了一套精密的动物实验,力求模拟临床情况并揭示深层机制。
实验选用了成年雄性SD大鼠,并采用Longa法建立了大面积脑缺血模型。
手术过程:在麻醉状态下,将尼龙线从大鼠颈外动脉插入,经由颈内动脉,阻断大脑中动脉的血液供应。术后第二天,使用5分制评分标准评估大鼠神经功能。只有出现提尾时前爪不能完全伸展、向瘫痪侧转圈等明确神经功能缺损症状(评分1-3分)的大鼠,被纳入后续实验。
成功建模的大鼠被随机分为两组:
CIMT组:从术后第7天开始,研究人员用石膏将大鼠的健侧(左侧)前爪固定在胸前,持续1、2或3周。这强迫大鼠在日常生活中只能使用其受损的(右侧)前爪进行移动、探索和进食(图1)。
对照组:不接受任何强制训练,让其自然恢复。

为了客观评估大鼠的运动功能恢复情况,研究者采用了两种方法:
诺达思的动物步态分析系统(CatWalk XT):这是一个评估自发行走啮齿类动物的步态分析系统。大鼠需要从一个装有玻璃板的通道中走过,高速摄像机从下方捕捉每一只爪子的精细脚印。本研究从众多参数中主要关注以下参数:时间足(初始双足支撑、末期双足支撑和站立持续时间)、比较足(支撑时相比)、动力足(身体速度)以及爪间协调(相位离散:对角线和同侧爪对)参数。
改良神经功能缺损评分:这是一套综合评分体系,从运动、感觉、平衡和反射四个方面评估神经功能缺损的严重程度,总分18分,分数越高代表缺损越严重。
4.顺行追踪
在术后第22-25天,研究者向大鼠双侧大脑的运动皮层注射了两种不同的腺相关病毒。在左侧运动皮层注射携带绿色荧光蛋白(eGFP)的病毒。在右侧运动皮层注射携带红色荧光蛋白(mCherry)的病毒。
这些病毒被神经元吸收后,会沿着神经纤维运输,从而将神经元投射出去的“线路”点亮。3周后,观察大鼠脑切片中红核区域,分别计数来自左右两侧运动皮层的绿色和红色荧光膨体。
为了从分子层面理解变化,研究者分别在术后第16天和第21天,提取了大鼠双侧红核的组织,进行了:
经过一系列严谨的实验,结果令人振奋,清晰地展示了CIMT带来的多重积极影响。
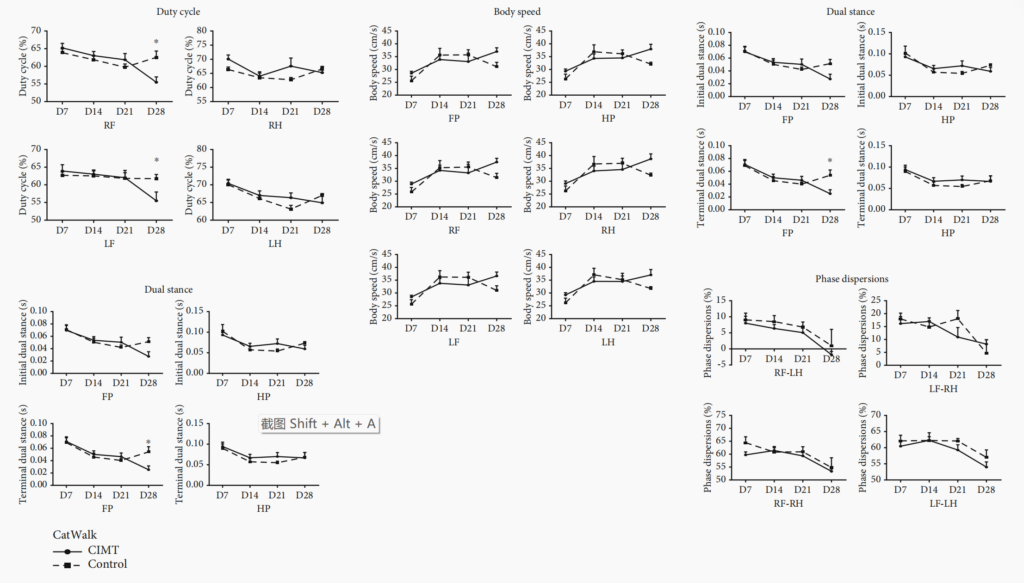
CatWalk步态分析:经过3周的CIMT训练后,与对照组相比,CIMT组大鼠的前爪功能显著改善。具体表现为:站立时间显著缩短,这意味着患侧前爪能更快地抬起和迈出下一步,支撑身体的能力更强。双足支撑时间显著减少,表明身体平衡和协调性更好。步态周期中的站立相比例降低,步态更接近正常大鼠。这些指标都直接指向了运动功能的提升(图2)。
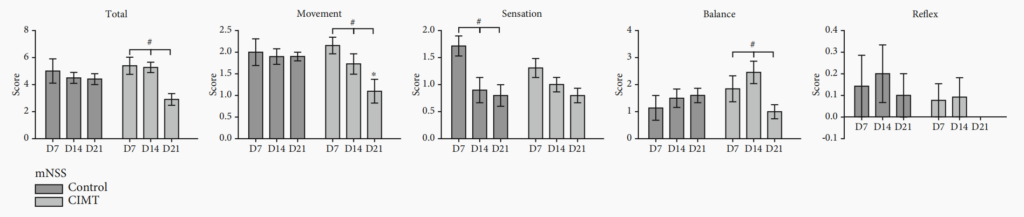
神经功能评分:CIMT组大鼠的总分、特别是平衡和运动实验的得分,在21天时显著优于对照组,且其自身得分也随着时间推移而持续改善。这表明CIMT不仅改善了行走,还增强了整体的平衡和协调能力(图3)。
Western Blotting 结果显示,在术后第21天,CIMT组大鼠健侧红核中的GAP43蛋白水平显著高于对照组。而损伤同侧的红核则无明显差异(图4a)。
免疫组化结果更直观地展示了这种变化。在术后第28天,CIMT组大鼠的双侧红核中GAP43的密度都显著高于对照组(图4b),并且健侧红核对整体增长的贡献更大。这强烈提示,CIMT首先激活了健侧红核的轴突生长,并可能在后期也影响到损伤侧,形成更广泛的神经重塑(图4a, b)。
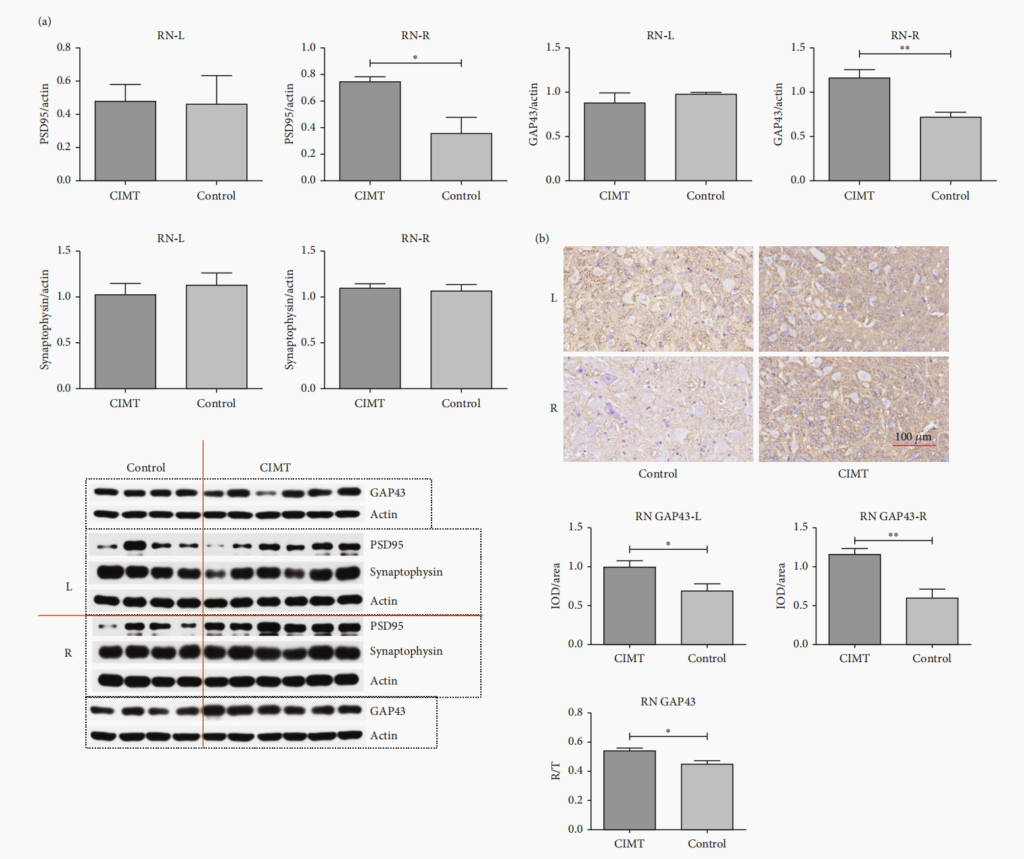
PSD95的表达变化:在术后第16天,Western Blotting检测发现,CIMT组大鼠健侧红核中的PSD95蛋白水平显著升高,而损伤侧红核无变化。这意味着,健侧红核神经元接收信息的能力在CIMT的刺激下被显著增强了。
突触素的表达:有趣的是,双侧红核的突触素水平在两组间并无差异。这可能意味着CIMT主要促进了轴突生长和突触后结构的重塑,而对突触前囊泡蛋白的影响可能需要更长时间或不同的干预强度才能显现。
结果显示,双侧投射增强:CIMT组大鼠来自健侧运动皮层(红色) 和损伤侧运动皮层(绿色) 向双侧红核的投射,其相对荧光强度(RN/CP比值)均显著高于对照组。
研究结果显示,在对照组红核区域,代表投射的荧光点稀疏;而在CIMT组,无论是红色还是绿色的荧光点都更加密集、丰富。这意味着CIMT不仅加强了损伤侧大脑向红核的指令输出,更神奇的是,它极大地促进了健侧大脑向双侧红核,特别是向健侧红核的投射,从而构建了一个更强大的、双侧协同的神经控制网络。
这项研究系统地揭示了在大面积脑卒中后,CIMT能够通过促进对侧(健侧)红核的神经可塑性,并增强双侧皮层-红核通路的投射,来代偿受损的运动功能。这为理解CIMT为何有效提供了重要的科学证据,也为寻找新的康复治疗靶点指明了方向——也许未来,结合药物或非侵入性脑刺激技术,靶向性地激活红核等皮层下结构,能与CIMT产生协同效应,为中风后功能障碍的患者带来更大福音。
Liu, Peile, et al. “Constraint‐Induced Movement Therapy Promotes Contralesional Red Nucleus Plasticity and Increases Bilateral Motor Cortex‐to‐Red Nucleus Projections After a Large‐Area Stroke.” Behavioural Neurology 2025.1 (2025): 3631524.
